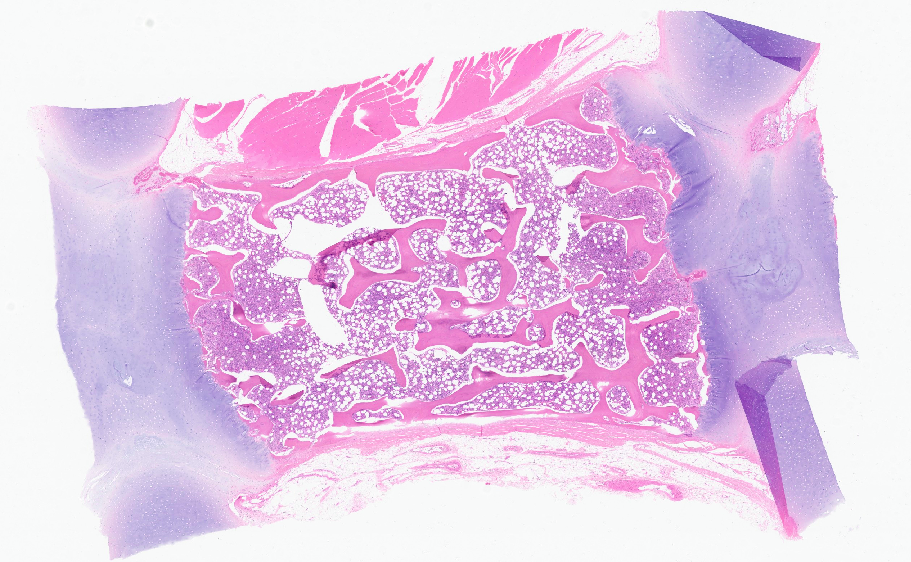
引 言
毒性病理学家在识别免疫系统变化方面发挥着关键作用,推动了免疫安全性的评定。生物疗法已经从简单地影响免疫系统转变为专门开发来调节免疫系统,这可能会影响毒性病理解释。,免疫调节疗法的爆炸性增长对毒性病理学家、毒理学家和监管审评员,在评估免疫系统变化的临床相关性和潜在不良反应方面提出了挑战。除了认识这些变化外,业界更期望评估、描述和解释免疫调节疗法和具有脱靶免疫毒性作用的非免疫调节药物如何影响复杂的免疫系统途径。在这篇专家论坛综述中,讨论了关于免疫系统评估的考虑、免疫调节疗法的现状、免疫毒理学(和免疫病理学)终点的简要概述、整合这些免疫安全性数据的重要性以及与评估不良反应的相关性。
免疫系统包括遍布全身的免疫器官和非免疫器官,这些器官共同作为一个完整的功能性免疫系统而发挥作用。免疫反应是高度动态和显著可变的,即使在非临床安全性研究中使用的传统实验室物种中,个体和群体之间也有一系常”反应。鉴于免疫系统的动态和可变性质,其评估不仅需要了解正常免疫反应,还需要了解辨别免疫调节是否反映了预期的、适应性的或病理性的能力。随着免疫调节疗法的显著增长,评估变得越来越复杂,这对毒性病理学家、免疫毒理学家和监管审评员在评估免疫系统变化的临床相关性和潜在不良反应方面提出了挑战。对免疫系统的治疗相关作用可包括从抑制到刺激的非特异性或特异性免疫相关作用。这些变化可能代表背景的增强、“正常”范围内的免疫变化、功能性或放大的药理学或明显的毒性。
早期的免疫毒理学评估主要集中于确定是否发生免疫抑制或免疫刺激以及发生的程度。然而,随着专门作用于靶向或调节免疫系统(表1)的疗法的出现,辨别免疫系统“毒性”的定义变得越来越困难。对于现代免疫毒理学评估,整合了免疫和非免疫器官中存在的一系列免疫测定(表型和功能)和组织病理学变化,以了解任何疗法或化学实体对免疫系统的影响。根据国际协调委员会(ICH)S8指南和提供人类药物标准免疫毒性评估信息的附加指南,可使用一组核心的体内和体外功能测试来评估免疫系统变化。
正是在这一背景下,免疫安全性的概念作为一个术语出现,用于描述供试品对免疫系统的广泛毒性或其他影响。免疫安全性评价整合了从发现到患者的非临床和临床数据,并解决了监管机构和公众在免疫系统效果和安全性管理方面对免疫安全性的风险。困难在于如何辨别预期的药理学何时转变为放大的药理学或毒性,以及这些毒性信号何时代表危害。此外,当免疫反应可能是针对治疗药物本身时,会出现额外的复杂性,如许多生物制剂(如抗药物抗体[ADAS]、免疫复合物沉积和超敏反应)。毒性病理学家越来越需要不仅能够识别免疫系统的变化,而且能够将免疫调节疗法对固有的免疫系统途径和反应的影响进行解释,并利用这些发现来应对不良反应。
免疫系统变化的不良反应评估建立在强调******实践和评估非临床安全性研究时要考虑的因素的一些出版文章上。这些立场文章表明,不良反应应以非临床研究为基础,在非临床研究中进行主要不良反应评估后考虑可转化性。这种逐步递进方法增加了对在动物模型中被认为是不利的病理发现的解释的清晰度,以及它是否可以被认为与人类相关。然而,新的免疫调节疗法在动物研究中的免疫系统发现,就其在预期人群中的相关性或预测性而言,评估起来极其复杂。评估不良反应的传统方法没有权衡可能影响免疫系统结果、解释的相关人类影响、药理活性、治疗适应症或感兴趣的患者群体。核心问题是,“病理学家如何在一个高度可变和反应灵敏的系统中,在对免疫系统有预期和治疗效果的情况下,做出不良反应决定?”
目前该问题的答案,将免疫变化的不良反应评估实际应用的方法、哲学和观点在整个行业中各不相同,特别是在免疫调节疗法的背景下。有些人会采取保守的做法,并评定任何符合Kerlin和Pandiri所述标准的免疫变化是不利的,即使是由于作用机制(MOA)所预期的。另一极端是那些认为任何目标药理学(从有意到放大)都不应被视为不利的人。然而,其他人会根据与其他免疫毒理学数据相结合的可观察的病理变化来综合评估来确定不良反应。最后,有些人会提出,在设计机理用于调节免疫系统的治疗的背景下评估免疫系统时,“什么是不利的?”可能不是正确的问题,并且最好描述免疫变化的范围。专业意见的这种可变性表明,在了解影响免疫系统评估的众多因素的情况下,开发一种一致的方法是必要的。我们认为,免疫结果的不良反应确定应保持灵活性,与情境相关,并结合证据权重(WOE)方法,最好是大量/特定的免疫毒理学相关结果。包括来自单独阶段报告8的任何可用的补充数据集。本文的目的是在当前免疫调节疗法的前景中,对确定非临床研究的不良反应所涉及的考虑因素进行讨论,希望未来国际和机构间的协调方法。
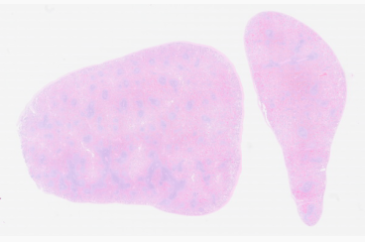
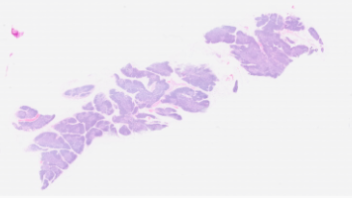
免疫系统和免疫系统变化的评估
理想情况下,免疫系统的综合评估包括确定形态学(即组织或细胞)、表型和功能变化,以及在正常免疫反应范围内将任何研究或患者相关变化置于该情境中。在非临床研究中,包括诱导、产生和分解动力学、动态免疫反应和试验样品特性(如MOA)的影响、研究设计、持续时间、评估时间点和免疫系统结果的评估技术在内的因素都被考虑在内。通常,血液学、临检、大体病理学、器官重量和组织病理学是标准毒性研究中免疫系统病理学评估的基础方面。对于病理学家来说,在常规评估过程中,通常会对有可能显示免疫系统变化的细胞和组织进行常规评估,这些细胞和组织通常足以识别常见的免疫变化,即使面向采用免疫调节疗法也是如此。然而,当需要进行更详细的评估时,无论是由于初始病理学评估的结果还是对复杂免疫变化的预期,免疫毒理学或增强组织病理学方法都可以提供有关免疫细胞亚群,通过免疫表型或通过功能性免疫毒理学终点的免疫反应变化。表2概述了一些用于鉴定免疫系统变化和表征免疫安全性的免疫毒理学(病理学和功能性)试验。
尽管免疫系统变化的功能评估最好使用免疫毒理学测定来确定,提示功能变化或与功能变化一致的免疫病理变化也经常观察到。组织病理学(传统的或增强的)的应用可以提供免疫应答变化的证据,支持抑制或刺激免疫应答或免疫应答的特定阶段。例如,细胞毒性疗法如顺铂和环磷酰胺通常减少免疫器官中的免疫细胞群(和其他高度增殖的细胞群),并可能对免疫应答产生功能性影响。针对特定免疫细胞群或途径的更具选择性的疗法可能会改变免疫器官的特定亚区,从而对功能产生影响。一个例子是靶向B细胞(用于自身免疫疾病)的疗法,其可以诱导生发中心减少和脾边缘区退化。免疫信号传导级联(如JAK/STAT途径)的抑制可能不会表现为免疫器官的形态学变化,但可能导致作为功能变化的支持性证据的间接效应,包括感染或其他临床效应(例如血栓栓塞或高脂血症)的发生率和/或严重程度增加。
相反,免疫刺激可能表现为炎症,或容易识别为免疫活性增强的结果,但可能更微妙,在“正常”变异范围内,甚至不存在。例如,免疫检查点抑制剂在癌症免疫治疗中取得了很大的成功,通过“释放免疫反应的制动器”来促进抗肿瘤免疫。在非临床研究中,这种增强可能表现为免疫器官细胞的轻微增加,但由于免疫/炎症反应增加,可能导致患者的免疫相关不良事件(IRAEs)。因此,IRAE可能通过实验动物的免疫反应来预测,也可能无法预测。显著的急性免疫刺激,如超敏反应或过敏反应,通常可导致死亡,仅有有限的临床诊断信息可用,并且很少或没有明显的解剖病理变化。最终,了解免疫反应、任何特定疗法的MOA以及潜在疗法(特别是针对免疫系统设计的疗法)如何改变免疫反应,有助于了解与研究动物物种和品系的免疫特异性相关的免疫系统发现的重要潜在不良反应。
免疫毒性是指对免疫(或其他系统)的结构、功能或成分的任何影响,导致免疫系统功能障碍。结果可能是宿主对感染性或肿瘤性疾病的防御能力下降(即免疫抑制)或免疫介导的损伤(如自身免疫、超敏反应或慢性炎症)。许多监管指南文件为免疫毒理学评估提供了有用的信息和基本框架,并提供了包括病理学在内的Woe方法,以确定毒性和评估风险。这些出版物提供了如下所述的有用信息:
· 评价免疫毒理学潜在风险的试验样品;
· 基于风险的评估和缓解方法
免疫或与免疫相关的不良反应;
· IRAE类别的类型信息(包括免疫抑制、免疫原性、超敏反应、自身免疫、不良免疫刺激、皮肤致敏和先天免疫效应);
· 免疫调节剂和其他相关术语的定义;
· 潜在免疫毒性的定义和特征
非临床研究中的发现;
· 用于鉴定和/或表征和/或鉴定患者群体中的IRAE的诊断标准;
· 关于实施Woe的有用建议
免疫系统安全测试方法。