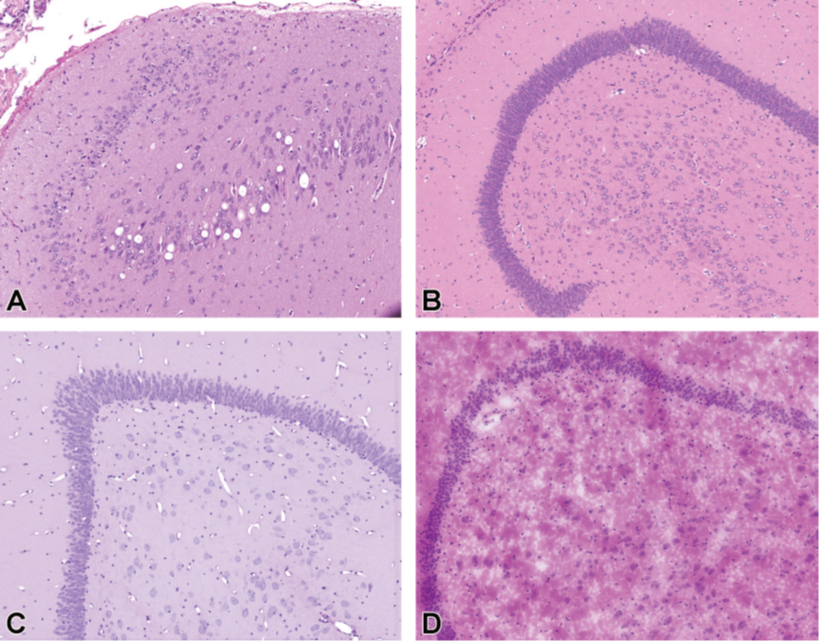
固定液对海马神经元空泡化的影响,其中非人灵长类动物通过鞘内途径给药6周剂量的5mg反义寡核苷酸(ASO)。
(A) 海马浸没固定在中性缓冲福尔马林(NBF)中,神经元出现大泡空泡化。相比之下,海马中没有观察到空泡化,浸没固定在Carnoy(B)中,灌注固定在改良的Karnovsky(C)中,或在冷冻切片检查的未固定冷冻组织中(D)
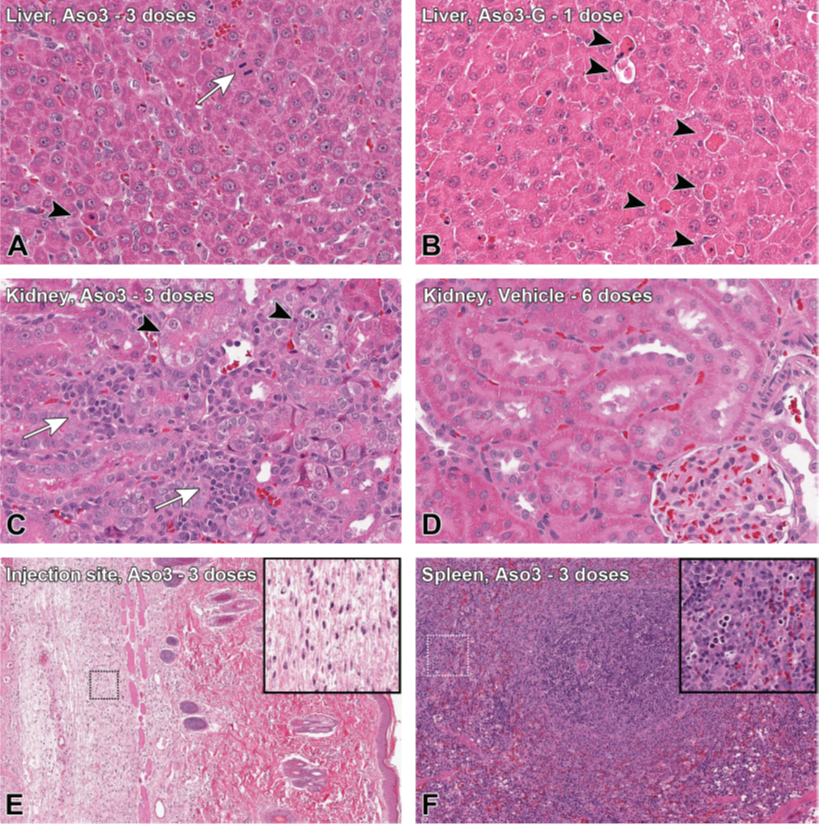
(A) 肝细胞有丝分裂(白箭头)和轻度凋亡/单细胞坏死(黑箭头), Aso3(毒理高剂量)40mg/kg. (B),严重凋亡/单细胞坏死(箭头),Aso3-G,20mg/kg.
(C)肾脏:肾小管变性(箭头)和单核炎性浸润(箭头),3剂Aso3(HT),40mg/kg .(D)肾脏:与用溶对照给药的大鼠未受影响的肾脏。
(E) 注射部位(皮肤、肩胛间区):单核炎性浸润.(F)脾脏:淋巴细胞凋亡和淋巴滤泡增生
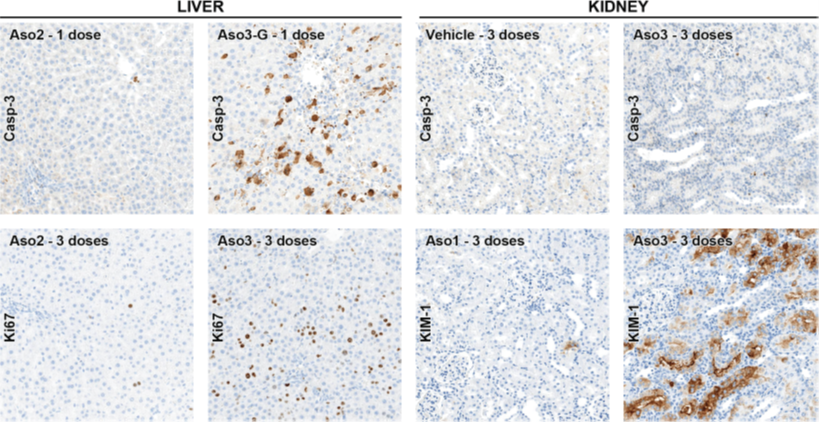
细胞死亡机制和增殖。Casp3、KIM-1的免疫组织化学染色实例
在给予Aso3-G毒理高剂量后,肝脏中观察到最高的Casp-3信号,表明细胞死亡是凋亡的机制。
然而,在肾脏中,ASO给药Casp与对照组大鼠相比,Casp-3的表达没有差异。
化合物(Aso3和Aso3-G)在给予HT的大鼠肝脏中观察到Ki67增殖细胞数量增加(主要在肝细胞中)。Aso3(HT)在近端肾小管上皮细胞中表现出最高的KIM-1信号,这表明肾小管坏死。
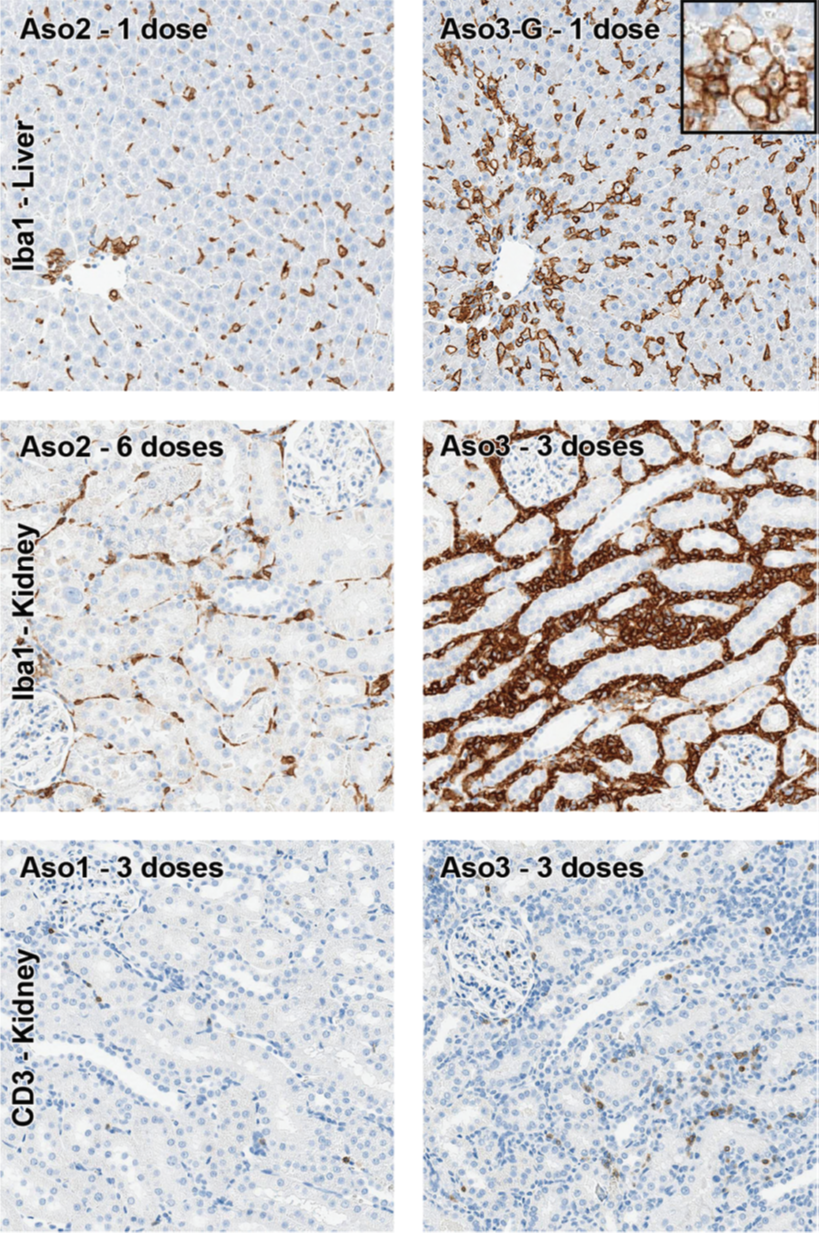
肝脏和肾脏中的炎性细胞。巨噬细胞(Iba1)以及T细胞(CD3)-免疫组织化学染色图片。
更高的Iba1细胞计数(枯否细胞)与HT ASO一起在肝脏中观察到,HT ASO。
插图代表凋亡小体被Iba1细胞吞噬。在肾脏中,Aso3(HT)的含量最高间质单核细胞浸润量,由大量巨噬细胞(Iba1)和较低比例的T淋巴细胞(CD3)
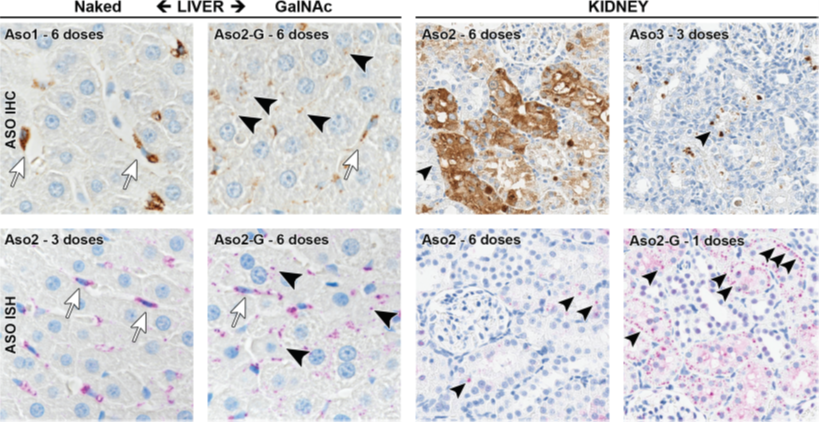
免疫组织化学(IHC)以及原位杂交(ISH))定位的代表性图片
含LNA的ASO在肝脏和肾脏中的积聚。在肝脏中,裸ASO主要积聚在枯否细胞中(箭头),在肝细胞内的水平非常低。
GalNAc偶联的ASO不仅在枯否细胞内积累(箭头),而且在肝细胞内也累积(箭头)。在肾脏中,所有LNAs主要在近端肾小管上皮细胞中积累,与它们的结合状态无关(箭头)
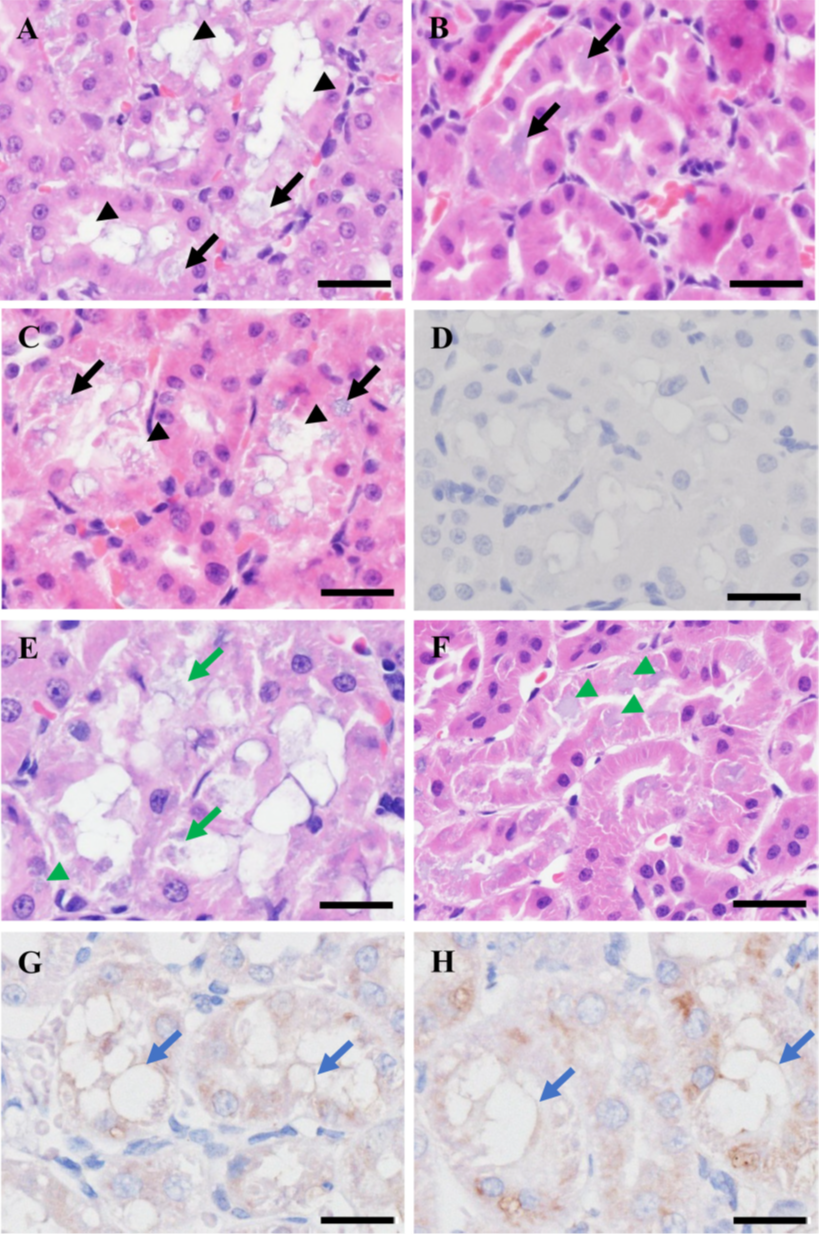
反义寡核苷酸(LNA-ASO)治疗组(ASO-2W)用(A)10%中性粒细胞缓冲液固定肾脏甲醛溶液(NBF)、(B)Karnovsky固定剂或(C)4%多聚甲醛磷酸盐缓冲液(PFA)。
(D) 免疫组织化学用10%NBF固定肾脏的ASO-2W肾损伤分子-1(KIM-1)染色。
1周LNA ASO治疗组(ASO-1W)用(E)10%NBF和(F)Karnovsky固定剂固定肾脏。免疫组织化学用10%NBF固定的肾脏的(G)ASO-1W和(H)ASO-2W的溶酶体相关膜蛋白2(LAMP-2)染色。
(A) 在近端小管中观察到嗜碱性粒细胞(黑色箭头)和空泡(黑色箭头。)(B) 未观察到空泡,但观察到嗜碱性颗粒(黑色箭头)。H&E染色。(C) 观察到嗜碱性颗粒(黑色箭头)和空泡(黑色箭头”)。。
(D)大多数空泡化近端小管是KIM-1阴性。(E,F)在近端小管中观察到的一些空泡含有微弱的嗜碱性颗粒(绿色箭头)。嗜碱性颗粒清晰可见,细胞结构得以保留(绿色箭头)。(G,H)空泡的膜表面对LAMP-2呈阳性(蓝色箭头)。
参考文献
Toxicologic Pathology 2018, Vol. 46(7) 735-745
NATURE COMMUNICATIONS | (2018) 9:723
Toxicologic Pathology 2021, Vol. 49(6) 1174-1192
Toxicologic Pathology, XX: 1-12, 2014
Toxicologic Pathology, XX: 1-10, 2015
Toxicologic Pathology2022, Vol. 50(2) 197–210
Toxicologic Pathology2021, Vol. 49(6) 1174-1192
艾联生物已完成多个小核酸药物的早期临床前开发阶段的药理药效和毒性病理评价,积累了大量的病理研究CRO服务经验